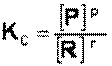Quatro fatores podem influenciar o equilíbrio de um sistema. São eles:
v Concentração
v Pressão
v Temperatura
v Catalisador
Obs.: A Temperatura é o único fator que além de deslocar o equilíbrio muda o valor de Kc ( Constante de equilíbrio). Lembrando que:
--------------------------------------------------------------------------------------------------------------
Concentração
Definições
o Um aumento em qualquer das concentrações resulta em um deslocamento de equilíbrio para o outro lado.
o A diminuição de alguma substância provoca o deslocamento para o seu lado.
o Durante as modificações, os valores de todas as concentrações são alterados, porém o valor de KC mantém-se o mesmo.
Sendo:
[R] = Concentração dos reagentes
[P] = Concentração dos produtos
[R] = equilíbrio se desloca para a direita
[R] = equilíbrio se desloca para a esquerda
[P] = equilíbrio se desloca para a esquerda
[P] = equilíbrio se desloca para a direita
Explicando
o Se aumentar a concentração de reagente, a reação precisa produzir mais quantidade de produto, por isso desloca-se para a direita.
o Se diminuir a concentração de reagente, a reação precisa produzir mais quantidade do próprio reagente, por isso desloca-se para a esquerda.
o Se aumentar a concentração de produto, a reação precisa produzir mais quantidade de reagente, por isso desloca-se para a esquerda.
o Se diminuir a concentração de produto, a reação precisa produzir mais quantidade do próprio produto, por isso desloca-se para a direita.
O equilíbrio é deslocado porque o Kc deve ser constante. Por isso, à medida que a concentração de um aumenta ou diminui a concentração do outro deve seguir de acordo.
Pressão (quando for gasoso)
Definições
o A pressão de um gás está associada ao seu volume.
o O aumento da pressão beneficia a reação com menor volume.
o A diminuição da pressão beneficia a reação com maior volume.
Sendo:
P = Pressão
V = Volume
Pressão =
Volume = Contração (volume diminui, portanto se contrai)
Pressão =
Volume = Expansão (volume aumenta, portanto se expande)
Explicação
o Aumento do volume do gás = EXPANSÃO
o Diminuição do volume do gás = CONTRAÇÃO
Seja a reação química:
Neste caso, o produto possui volume (2volumes) e os reagentes possuem volume (4volumes). Assim quando a pressão aumentar o equilíbrio vai se deslocar para onde tiver menor volume para que o Kc se mantenha constante. Nesse caso deslocará para direita, onde está o produto, que têm menor volume.
Explicação
o Para verificar o volume do reagente e do produto, basta olhar o número de mols que eles possuem reação química.
o Com um aumento da pressão, o equilíbrio será deslocado para o sentido que tem menor volume.
o Com a diminuição da pressão, o equilíbrio será deslocado para o sentido que tem maior volume.
Temperatura
Definições
o É a única alteração que pode modificar o valor da KC.
o O aumento da temperatura beneficia a reação endotérmica (ganha calor). Essa reação é beneficiada porque quando há o aumento da temperatura ela absorve parte desse calor, a fim de minimizar os efeitos. Deslocamento ocorre em sua direção.
o A diminuição da temperatura beneficia a reação exotérmica (libera calor). Essa reação é beneficiada porque quando há a diminuição da temperatura ela fornece (libera) calor para o sistema, a fim de minimizar os efeitos. Deslocamento ocorre em sua direção.
Catalisador
Definições
o Catalisador = substância química que acelera a reação química
o A presença de um catalisador não altera o valor da Kc.
o O catalisador promove a diminuição do momento do equilíbrio. Altera tanto na reação direta como na reação inversa.
Resumo de Deslocamento de Equilíbrio Químico
| Perturbação Externa | Deslocamento do Equilíbrio | Alteração de Kc ou Kp |
| Adição de um participante | No sentido oposto ao do participante | Não |
| Retirada de um participante | No sentido do participante | Não |
| Aumento da pressão total | No sentido do menor volume | Não |
| Diminuição da pressão total | No sentido do maior volume | Não |
| Aumento da temperatura | No sentido endotérmico | Sim |
| Diminuição de temperatura | No sentido exotérmico | Sim |
| Presença de catalisador | Não | Não |
Leia mais sobre Le Chatelier - Recomendado por Resumo Escola